В дополнение к уже упомянутым видам бактерий из организма матери через плаценту мы получаем защитные антитела. С их помощью, а также под патронатом пока еще малочисленной, но отважной армии собственных бактерий мы готовы появиться на свет. Но сам процесс рождения тоже не так-то прост. Ведь и он имеет значительные последствия для нашего микробиома, которые еще долго будут сказываться на нашей дальнейшей жизни.
Рождение
При нормальных родах во время выхода из родового канала голова ребенка обращена лицом к прямой кишке матери. Такое положение означает, что нос и рот новорожденного оказываются в непосредственном контакте с содержимым влагалища и прямой кишки. Разве есть лучший способ получить "прививку" таким количеством бактерий, чем оказаться лицом к лицу с их источником! В журнале Proceedings of the National Academy of Sciences были опубликованы результаты исследований, которые показывают, что дети, рожденные естественным путем, уже имеют в своем организме достаточно разнообразных лактобактерий наряду с прочими "хорошими" микробами, в то время как появившиеся на свет в результате кесарева сечения в среднем получают заметно большее количество "плохих" больничных бактерий (вроде стафилококка), обычно ассоциирующихся с инфекциями и болезнями.
Быстрый глоток материнских микроорганизмов при появлении на свет дарует нам такие преимущества, в которые даже трудно поверить. Бактериальная "прививка" в самый первый момент нашего бытия оказывается важнейшим шагом в становлении иммунной системы. В результате кесарева сечения этот шаг выпадает, поэтому операция нередко связана с возникновением у ребенка астмы, аллергии, излишнего веса, диабета первого типа и других аутоиммунных заболеваний. В главе 3 мы более подробно рассмотрим значение бактерий для организма новорожденного в первые секунды жизни, а также современные напасти, вызванные отсутствием такого воздействия или его недостаточностью.
Грудное вскармливание
Олигосахариды – это треть состава грудного молока, несмотря на то что новорожденный абсолютно не способен их переваривать. Их задача не в том, чтобы накормить младенца, а в том, чтобы предоставить питательные вещества бактериям, уже присутствующим в его организме. Особенно бифидобактериям, которые подавляют стафилококки и другие болезнетворные микробы, присутствующие на сосках матери, так что они входят в микробиомный арсенал ребенка на правах главного действующего лица. И пока бифидобактерии активно поглощают олигосахариды, лактобактерии кишечного тракта новорожденного участвуют в расщеплении других углеводов, а также прочих усваиваемых компонентов грудного молока, – это превосходный пример симбиоза человека и микроорганизмов.
По статистике, в США у грудничков на 20 % больше шансов выжить по сравнению с искусственниками. В главе 7 мы обсудим тревожную тенденцию к увеличению числа искусственников и рассмотрим, как некоторые современные медицинские (и не только) практики сказываются на микробиоме человека.
Младенчество
Практически все, с чем взаимодействует младенец, завершает свой путь у него во рту. На данном этапе его жизни это один из главных способов познания внешнего мира. Таким же образом внешний мир взаимодействует с микробиомом ребенка, в результате чего бактерии, присутствующие в доме, в организме брата, сестры или домашнего питомца, получают доступ к его желудочно-кишечному тракту. Подобное внешнее воздействие тренирует его иммунную систему, учит ее отличать друзей от врагов. И факторы вроде размера семьи, качества питания и воды оказывают огромное влияние на правильное развитие микробиома ребенка.
Неудивительно, что микробиом младенца наиболее близок к микробиомам его родственников, особенно к материнскому. Однако эта система очень подвижна, постоянно перестраивается и эволюционирует, разнообразие видов микроорганизмов непрерывно растет, и изменение привычек в питании, высокая температура или курс антибиотиков могут иметь серьезные последствия для нее. Через несколько недель после рождения бактерии в организме младенца обретают все большую специализацию, а в течение нескольких месяцев число видов населяющих его микроорганизмов начинает возрастать – примерно от сотни в грудном возрасте до тысячи и более к моменту взросления.
От детства ко взрослой жизни
К трем годам микробиом формируется почти полностью и уже напоминает микробиом взрослого человека, хотя важнейшие возрастные изменения (половое созревание, начало менструации, беременность и менопауза) всегда вызывают серьезные подвижки в его составе. Ряд физиологических процессов, связанных с половым созреванием (увеличение секреции сальных желез – распространенная причина образования прыщей или более резкий запах пота), на самом деле является результатом изменений бактериального фона организма в зависимости от того, какие виды микроорганизмов доминируют.
К старости мы утрачиваем это разнообразие бактерий, поэтому микробиом становится все менее индивидуальным и все более походит на микробиомы наших сверстников. Изменения в микробиотическом составе продолжаются, но по мере нашего старения микробиом стабилизируется и приобретает тенденцию к восстановлению прежнего состояния после атак вроде инфекции и курса антибиотиков.
Обновление
Наша жизнь начинается в утробе матери, там мы абсолютно свободны от каких-либо микроорганизмов, но в конце концов мы получаем их триллионы. А что происходит с ними после нашей смерти? Интересно заметить, что нет никакого круговорота микробиома, он умирает вместе с нами. И каждое последующее поколение микробов проходит свой жизненный цикл с нуля до многочисленного царства внутри нашего организма и хорошо (будем надеяться) адаптируется к условиям конкретного поколения.
Разнообразие видов необходимо для баланса экосистемы во внешнем мире, но это также справедливо и для микроскопической среды внутри нас. К сожалению, современность делает обеднение мира микробов частью общего наследия цивилизации; уменьшение разнообразия этого мира из поколения в поколение – результат медикаментозного лечения, чрезмерно переработанных продуктов питания и нашего сверхобеззараженного образа жизни. Организм современного человека служит домом примерно лишь для двух третей от того количества видов микроорганизмов, которые обитают в теле индейца из дебрей Амазонки, ни разу не испытавшего воздействия антибиотиков. Как мы увидим во второй части книги, восстановление этой недостающей трети микробов – серьезная задача, требующая усилий и настойчивости.
Не существует идеальных микробиомов, но некоторые их типы очевидно являются более здоровыми по сравнению с другими, несмотря на колоссальные различия. Цель The Human Microbiome Project ("Проекта по исследованию человеческого микробиома") и других подобных исследований – понять, что можно считать "нормальным" микробиомом современного человека. Это смелое предприятие, учитывая скорость, с какой меняется микробиотический ландшафт. Компании вроде uBiome позволяют каждому вести "научный" журнал поведения своей микрофлоры, сравнивать эти данные с данными других людей, а также отслеживать реакцию своих микроорганизмов на изменение привычек и режима питания.
Изучение человеческого микробиома способно стать новым передовым направлением в медицине. В результате, возможно, появятся ответы на вопрос, почему мы болеем, и обнаружатся новые способы самолечения. В следующей главе мы узнаем, чем же на самом деле занимаются кишечные бактерии помимо производства газов и почему они так важны для нашего здоровья и хорошего самочувствия.
Глава 2. Микробы: ваши рабочие пчелы
Представьте, что ваше тело – это фабрика. Легкие, печень, почки – это станки, которые обеспечивают работу всего производства: извлечение кислорода, фильтрацию крови, удаление токсинов, синтез гормонов и еще много чего сложного, что делает нас живыми существами. Некоторые процессы на этой фабрике реализуются на автомате, но в большинстве своем эти "сборочные конвейеры" требуют постоянного контроля, наблюдения, обслуживания и настройки.
Наш организм является вместилищем для всех этих станков и механизмов, но кто работает на них? Как происходят сложнейшие процессы, например пищеварение? Кто помогает расщеплять пищу и кто определяет, что подлежит поглощению, а от чего необходимо избавиться? Каким образом организм распознает грозную инфекцию и отличает ее от колонии безобидных бактерий? Кто посылает сигнал иммунной системе: мобилизовать войска и дать отпор врагу или проигнорировать безвредного нарушителя, который не представляет никакой опасности?
Это все делают наши микробы! За миллионы лет эволюции мы стали домом для многочисленной армии микроскопических рабочих, которые сами подрядились помогать нашему телу выполнять его функции. Они производят нужные организму вещества, которые по тем или иным причинам он сам производить не может. В войне с нашими врагами они занимают нашу сторону. Они активируют те из наших генов, которые нам нужны, и деактивируют те, в которых мы не заинтересованы. Взамен мы предоставляем всему этому войску стол и кров.
Будучи их хозяевами, мы жизненно необходимы им, поэтому наше благополучие для них приоритетно. Однако при определенных обстоятельствах они способны ополчиться против нас и спровоцировать большую беду: инфекцию и даже рак. Наших микроскопических сожителей можно классифицировать на три основные группы:
1) бактерии-комменсалы, которые извлекают пользу из взаимоотношения с хозяином, а хозяин при этом не получает ни пользы, ни вреда;
2) симбиотические организмы (еще их называют мутуалистами), которые помогают поддерживать нам свое здоровье;
3) патогенные микроорганизмы (известные как "оппортунистическая флора"), которые способны причинить нам вред.
Настоящие джунгли
Большинство человеческих бактерий можно отнести к четырем типам – актинобактерии, фирмикуты, протеобактерии и бактероиды, – каждый из которых состоит из множества видов. В разных отделах нашего организма присутствуют бактериальные общины, различные в зависимости от условий обитания (кислород, мокро́та, кровоток).
Анаэробные микробы, для жизнедеятельности которых не нужен кислород, в основном встречаются в кишечнике. Стафилококки лучше всего чувствуют себя на коже, а вот стрептококки, которые также участвуют в производстве швейцарского сыра, селятся в ротовой полости и верхних дыхательных путях. Все эти бактерии существуют в патогенных (то есть болезнетворных) формах, но те из них, что населяют наш организм на постоянной основе, по большей части безвредны, особенно если их рост и развитие ограничивает адекватное количество других участников симбиоза.
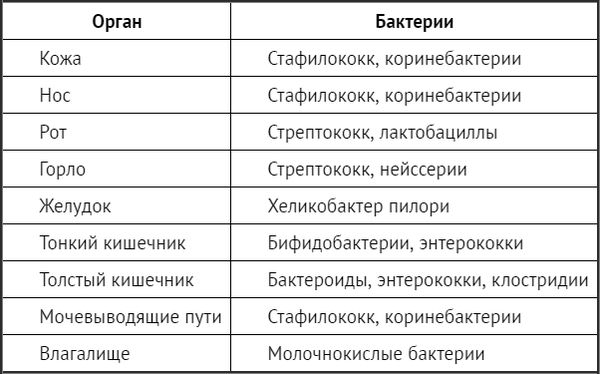
Таблица 2.1. Основные бактерии, населяющие тело человека
В зависимости от состава кишечной микрофлоры люди делятся на три энтеротипа. В 2011 году исследователь Пер Борк предложил следующую классификацию: первый тип характеризует преобладание бактероидов, второй – превотелл при незначительном количестве бактероидов, а третий – руминококков. Соответствие каждого человека тому или иному энтеротипу никак не связано с возрастом, полом, национальностью, однако зависит от длительных привычек в питании. Западная кухня, богатая белками и животными жирами, как правило, ассоциируется с первым энтеротипом и преобладанием бактероидов. Второй энтеротип (преобладание превотелл) характерен для тех, кто потребляет много углеводов, особенно пищевые волокна (клетчатку, лигнин, пектин).
Разделение на энтеротипы связано с предрасположенностью к определенным нарушениям, например к ожирению, различным воспалениям и раздражениям. Это лишь подтверждает гипотезу, что пища существенно влияет на ваше самочувствие и состояние здоровья. Возможно, в будущем мы научимся подбирать диеты для разных энтеротипов, а также синтезировать максимально эффективные пробиотики в зависимости от состава нашей микрофлоры.
Что делают кишечные бактерии?
Симбиотические микроорганизмы – это "хорошие" бактерии, которые выполняют множество очень важных функций. Они способствуют пищеварению, сохраняют целостность слизистой оболочки кишечника (выстланная эпителием поверхность, которая служит барьером между содержимым кишечника и полостью тела), борются с вредными микробами, а также участвуют в тренировке нашей иммунной системы и помогают ей отличать врагов от друзей. Они расщепляют сахар, преобразуя его в короткоцепочечные жирные кислоты, таким образом питая клетки кишечника. Они синтезируют множество энзимов, витаминов и гормонов, которые наше тело не способно вырабатывать самостоятельно. Кишечная микрофлора измельчает пищу на те составные части, которые могут быть полностью усвоены нашим организмом. Это значит, что, даже если вы придерживаетесь суперздоровой и насыщенной полезными ингредиентами диеты, без достаточного количества "правильных" кишечных бактерий ваш организм будет не в состоянии принять все те витамины и другие питательные вещества, которые содержатся в пище.
Функции кишечных бактерий
• преобразуют сахар в короткоцепочечные жирные кислоты – источник энергии;
• вытесняют из организма патогенные микробы;
• способствуют пищеварению;
• помогают организму усваивать питательные вещества (кальций и железо);
• поддерживают кислотно-щелочной (pH) баланс;
• поддерживают целостность слизистой кишечника;
• способствуют усвояемости лекарств;
• регулируют гены;
• нейтрализуют канцерогенные вещества;
• производят пищеварительные энзимы;
• синтезируют витамины группы B (тиамин, фолиевую кислоту, пиридоксин);
• синтезируют жирорастворимые витамины (витамин K);
• синтезируют гормоны;
• тренируют иммунную систему и помогают ей отличать друзей от врагов.
Большинство кишечных бактерий анаэробные, то есть благоприятная для них среда обитания или содержит мало кислорода или не содержит его вовсе. По мере продвижения вниз по желудочно-кишечному тракту концентрация бактерий возрастает – желудок и тонкий кишечник обладают значительно меньшим количеством бактерий, чем толстый кишечник. Некоторые виды бактерий делают свое дело среди клеток, выстилающих внутреннюю поверхность кишечника, другие проходят сквозь него транзитом, выполняя свои функции, размножаясь и в конце покидая организм со стулом.
Регулирование иммунной системы
Пищеварение не единственный процесс внутри организма, для которого присутствие кишечных бактерий критично. Сам факт, что потенциально мы беззащитны перед целым сонмом микробов – и "хороших" и "плохих", – играет ключевую роль в становлении, развитии и тренировке нашей иммунной системы. В результате эта система обретает способность отличать безвредные инородные организмы (и просто их игнорировать) от опасных патогенных, на агрессию которых необходимо давать быстрый ответ. В главе 7 мы увидим, что случается, если окружить себя суперобеззараженной средой, где совершенно отсутствуют необходимые для здоровья ранние контакты с микроорганизмами.
Модулирование генов
Геном человека состоит примерно из 23 тысяч различных генов, а генов различных микроорганизмов в сумме более 8 миллионов. Широкомасштабные исследования нашего микробиома доказывают, что особенности генетической структуры населяющих нас кишечных бактерий играют заметную роль. Они фактически дают инструкции жизненно важным процессам, например усвоению углеводов или детоксикации. Надо особо подчеркнуть, что эти инструкции отсутствуют в геноме человека. Бактерии также способствуют проявлению либо, наоборот, подавлению генов некоторых наследственных болезней в зависимости от внутреннего состояния организма (то есть от собственной среды обитания) и генетической предрасположенности человека к определенным недугам. Бактериальное модулирование генов объясняет, почему во многих случаях наследственные болезни неодинаково влияют на членов одной семьи, даже на однояйцевых близнецов: они обладают одинаковыми генами, но разными микробиомами.
Вы здоровы, пока здоровы ваши кишечные бактерии
Замечали ли вы, что некоторые люди никогда не болеют, даже когда у всех течет из носа, когда все кашляют и гриппуют? Эти индивиды подвержены воздействию опасного вируса, как и остальные, но их здоровый микробиом, в котором присутствует множество важных бактерий, способен вытеснять своих патогенных собратьев, оставаясь при этом в добром здравии. Антибиотики могут сделать вас даже более восприимчивыми к инфекциям, так как они разрушают, в частности, и полезные виды бактерий, естественных врагов болезнетворных микробов и вирусов. В ходе недавних исследований бактериальные белки были введены мышам, зараженным ротавирусом, который сопровождается тяжелейшим желудочно-кишечным расстройством, уносящим жизни полумиллиона детей в год по всему миру. В результате таких инъекций подопытные мыши исцелялись от вирусной инфекции. Те же белки показали свою эффективность в борьбе с другими вирусами, включая даже грипп, что демонстрирует, какую важную роль играет бактериальная микрофлора в защите от вирусных атак.
Здоровье нашего микробиома – один из факторов, определяющих, кто выживет в условиях распространения смертельно опасных вирусов. В группе риска оказываются самые маленькие дети, чей микробиом еще не сформировался, и самые пожилые люди, у которых популяция полезных бактерий представлена меньшим числом и меньшим разнообразием видов. Злоупотребление антибиотиками также приводит в группу повышенного риска, так как эти препараты убивают всех подряд – и патогенные, и полезные микроорганизмы. Конечно, в восприимчивости к вирусным атакам играют свою роль и другие факторы: уже имеющиеся проблемы со здоровьем, то, насколько вы закалены, правильно ли питаетесь и так далее. Однако все это сложным образом связано с состоянием микробиома. Поэтому можно сказать, что наличие "хороших" бактерий в достаточном количестве – залог надежной защиты организма и от острых, и от хронических болезней.
Эллисон обратилась ко мне с жалобами на постоянные запоры и вздутие живота. Несмотря на то что состояние пищеварительной системы значительно улучшилось после добавления в рацион растительных волокон, ее продолжал беспокоить хронический синусит. Каждый раз, когда Эллисон оказывалась у меня на приеме, она либо только приступала к очередному курсу антибиотиков, либо заканчивала его. Причем было ощущение, что чем больше антибиотиков она принимает, тем отчетливее и сильнее проявляются все симптомы инфекции. Мы подробно рассмотрим тяжелое негативное воздействие антибиотиков на микробиом в главе 4.
Осознание, что инфекцию вызывает скорее бактериальный дисбаланс, а не конкретный патогенный микроорганизм, помогло нам подобрать методы лечения. Внутри нас живут организмы, неконтролируемый рост которых может привести к проблемному их соотношению. Решение заключается не в тотальном уничтожении всего и вся – ведь вместе с "плохими" микробами погибают колонии полезных бактерий. Мы восстанавливаем баланс микрофлоры и популяции "хороших" бактерий, изменяя режим питания, образ жизни, делая его благоприятным для микробиома и поддерживая его тщательно подобранными пробиотическими препаратами. Мой план "Долой чистоту" подскажет, как достичь этой цели, поможет решить давние проблемы со здоровьем и предотвратить появление новых.