Хронический ДВС-синдром надо отличать от гиперкоагуляционного синдрома, который способствует развитию ДВС-синдрома, но принципиально отличается от него как патогенетически, так и по клиническим и лабораторным данным. Гиперкоагуляционный синдром есть повышенная готовность к свертыванию крови, компенсированная противосвертывающими механизмами. Поэтому при нем нет ни локальных, ни диссеминированных тромбов в сосудистой системе, в то же время быстро формируется сгусток крови в пробирке, при этом он рыхлый, укорочено время свертывания крови по Ли – Уайту, повышены агрегационные показатели тромбоцитов в ответ на добавление различных агонистов (ристоцетин, АДФ, коллаген, арахидоновая кислота), удлинен фибринолиз. Самочувствие при гиперкоагуляционном синдроме чаще всего может оставаться хорошим, хотя иногда появляются некоторые отклонения: "тяжесть в голове" и головные боли, быстрая утомляемость, кровь при взятии из вены сворачивается в игле; в местах пункции вены легко тромбируются – выходят "из строя". Причинами формирования и поддержания в определенных временных рамках гиперкоагуляционного синдрома являются, с одной стороны, стимуляция и активация механизмов, направленных на усиление свертывания крови, а с другой стороны, активация противосвертывающих систем.
По патофизиологическим механизмам и патогенетическим особенностям в гиперкоагуляционном синдроме можно выделить ряд основных форм: а) гиперкоагуляционный синдром при полиглобулии характеризуется наличием избытка клеток в циркуляторном русле (эритроцитозы и гипертромбоцитозы), что приводит к стазам крови преимущественно в системе микроциркуляции; дальнейшее сгущение крови, например спровоцированное диуретиками, может привести к тромбозам и ДВС-синдрому; б) гиперкоагуляционный синдром при гематогенных тромбофилиях, т. е. при определенных дефектах клеточных и плазменных элементов свертывания крови, может наблюдаться при дефиците AT III, аномалии системы протеина С, мутантном V факторе Leiden, гипергомоцистеинемии, мутантном протромбине 20210A, наличии волчаночного антикоагулянта – аутоантител к фосфолипидам, синдроме "липких тромбоцитов", резком повышении уровня фактора Виллебранда и активности VIII фактора; в) гиперкоагуляционный синдром при травматизации или нарушении целостности сосудистой стенки сопровождается формированием тромба, однако он строго локализован, и в системе гемостаза при этом может наблюдаться развитие гиперкоагуляционного синдрома, а не только активный местный тромбоз; именно поэтому в этой группе больных может осуществляться быстрый переход гиперкоагуляционного синдрома через короткую фазу гиперкоагуляции диссеминированного внутрисосудистого свертывания в гипокоагуляционную фазу ДВС-синдрома; кроме того, при наличии длительного локального кровотечения, развивающегося при неполноценной остановке кровоточивости – неполноценном тромбозе (язвенная болезнь желудка и двенадцатиперстной кишки, неспецифический язвенный колит и другие формы патологии), "зияющие сосуды" с кровоточивостью всегда будут сопровождаться гиперкоагуляционным синдромом и, как следствие, при этих формах патологии легко осуществляется переход гиперкоагуляционного синдрома в острый ДВС-синдром; г) гиперкоагуляционный синдром вследствие изменений гемостаза при различного рода тромбоцитопенических состояниях (апластическая анемия); д) гиперкоагуляционный синдром при опухолях, которые, являясь по площади поражения небольшими, сопровождаются формированием выраженных признаков гиперкоагуляционнного синдрома вследствие клеточного распада и выброса в кровь тканевого тромбопластина.
Клиническая картина и диагностика. Клиническая картина складывается из симптомов основной патологии и синдрома диссеминированного внутрисосудистого свертывания. При остром течении гиперкоагуляционная фаза может быть затяжной, но может протекать быстро и в считаные минуты смениться гипокоагуляцией. При гиперкоагуляционной фазе острого ДВС-синдрома выявляется повышенное потребление факторов свертывания, тромбоцитов, адгезивных молекул (фибриногена, фибронектина), первичных антикоагулянтов-антипротеаз (антитромбина III, протеина С) и компонентов системы фибринолиза (плазминогена, тканевого активатора плазминогена и др.). Принципиальное отличие гиперкоагуляционного синдрома от гиперкоагуляционной фазы ДВС заключается в отсутствии признаков полиорганной патологии и потребления факторов свертывания; фибринолитическая активность снижена и повышена агрегация тромбоцитов, визуально образование сгустка крови в пробирке ускорено. Гипокоагуляционная фаза острого ДВС-синдрома характеризуется лабораторными маркерами потребления (сгусток в пробирке либо не образуется, либо он рыхлый и быстро растворяется). Выражен диффузный геморрагический диатез (кровоточивость гематомно-петехиального типа): появляются петехии и экхимозы в местах инъекций, наложения манжетки тонометра, в местах механического трения, кровотечение из операционной раны, метроррагии (при акушерскогинекологической патологии), носовое и желудочно-кишечное кровотечения, кровоизлияния в кожу, слизистые оболочки, паренхиматозные органы. В результате кровоизлияния в надпочечники возможно развитие острой надпочечниковой недостаточности.
При массивной кровопотере ДВС-синдром развивается вследствие уменьшения объема циркулирующей крови, падения артериального давления с последующим развитием стойкой гипотонии, гипоксии, появлением признаков полиорганной недостаточности и метаболического ацидоза. Организм отвечает на массивную кровопотерю спазмом периферических сосудов (развивается централизация кровообращения), выбросом в сосудистое русло эритроцитов из депо (селезенка, кожа, мышечные капилляры) и увеличением объема циркулирующей плазмы. Вследствие гемодилюции улучшается текучесть крови, снижается ее вязкость. Если при этом значительно уменьшается мышечная активность, то сокращается потребность организма в объеме циркулирующей крови и потребность в кислороде. Увеличиваются частота дыхания, сердечный выброс, улучшается отдача кислорода в тканях и его утилизация, происходит перераспределение органного кровотока, в результате которого доставка кислорода обеспечивается в "порядке важности": сердце, легкие, головной мозг, печень, почки. Кроме того, очень часто острая массивная кровопотеря происходит у больных, исходно имеющих нарушения в системе свертывания, обусловленные наличием опухоли, инфекции, дефектов в клеточном или плазменном составе крови или сосудистой стенки. Нередко эти нарушения проявляются формированием гиперкоагуляционного синдрома, наличие которого определяет тяжесть течения синдрома острой массивной кровопотери, трансфузиологическую тактику ее восполнения и предупреждения развития острого ДВС-синдрома. Необходимо подчеркнуть, что причиной гибели больных при острой массивной кровопотере является не столько потеря кислородоносителя – гемоглобина, компенсируемая обездвиженностью и подключением кислорода в носовые катетеры, сколько развитие ДВС-синдрома. В табл. 7 приведены основные дифференциальнодиагностические признаки гиперкоагуляционного синдрома и обеих фаз ДВС-синдрома.
Дифференцировать гиперкоагуляционный синдром и гиперкоагуляционную фазу ДВС-синдрома можно клинически. Если у больного появляются признаки полиорганной патологии, даже не очень резко выраженные, – заторможенность, односложность и быстрая истощаемость в ответах на вопросы, глухость тонов сердца, участки бронхиального дыхания в легких, небольшое увеличение печени, снижение диуреза и появление протеинурии и цилиндрурии, снижение перистальтики кишечника, – все вместе взятое неопровержимо свидетельствует о развитии гиперкоагуляционной фазы синдрома ДВС крови. Эта фаза в отличие от гиперкоагуляционного синдрома является смертельно опасной патологией, которую необходимо интенсивно лечить прежде всего переливанием свежезамороженной плазмы.
Таблица 7. Признаки гиперкоагуляционного синдрома и различных фаз ДВС-синдрома
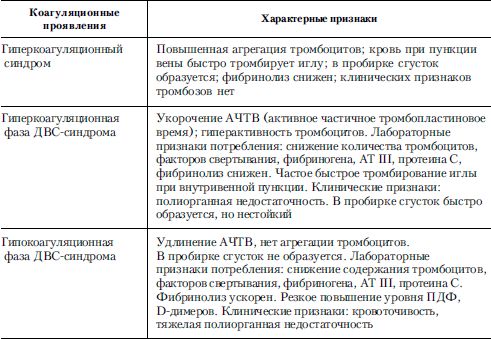
Следует еще раз подчеркнуть, что незамеченный вовремя гиперкоагуляционный синдром, который не имеет специфической клинической картины, очень быстро может перейти в гиперкоагуляционную фазу синдрома ДВС, а затем, в достаточно короткий срок, в гипокоагуляционную фазу ДВС-синдрома с ее неуправляемым потреблением в многочисленных микротромбах тромбоцитов, плазменных факторов свертывания, нарушением равновесного состояния между системами свертывания и фибринолиза, что клинически проявляется тотальной кровоточивостью и рецидивами органных кровотечений.
Лечение. При полиглобулии, характеризующейся наличием избытка эритроцитов и/или тромбоцитов в циркуляторном русле, проводится непосредственная терапия основного заболевания. При эритремии необходимо проводить эритроцитаферез. Гиперагрегабельность тромбоцитов требует назначения антиагрегантов (аспирин, тиклид, плавикс), при наличии гиперкоагуляции (укорочено АЧТВ, удлинение фибринолиза) проводят лечение низкомолекулярными гепаринами (фраксипарин, клексан или фрагмин). По показаниям (прогрессия опухолевого роста) назначаются цитостатики. При проведении эритроцитафереза пациенту вводится гепарин и назначаются антиагреганты (преимущественно аспирин).
При патологии иммунных комплексов эффективны антиагреганты, низкомолекулярные гепарины и различные варианты плазмафереза. При аутоиммунной агрессии (системная красная волчанка и др.) наряду с использованием стероидных гормонов эффективна терапия гепарином, антиагрегантами, плазмаферезом. Гиперкоагуляционный синдром при аутоиммунном веновенулите удается нивелировать путем сочетания внутривенного введения нефракционированного гепарина, антиагрегантов (тиклид или плавикс), стероидных гормонов (дексаметазона) и цитостатиков (винкристин, циклофосфан).
Гиперкоагуляционный синдром при атеросклеротическом повреждении сосудов (часто коронарных артерий) наряду с традиционной терапией ишемической болезни сердца (нитраты, (3-блокаторы, антагонисты кальция и др.) требует применения антиагрегантов (аспирин, тиклид, плавикс), иногда их комбинаций (аспирин + плавикс) в адекватных дозах. Исследование агрегационных показателей тромбоцитов должно показать заблокированность агрегации тромбоцитов (отсутствие второй волны агрегации и наличие феномена дезагрегации тромбоцитов). Кроме того, пациенты должны получать антикоагулянтную терапию; предпочтение отдается пероральным препаратам – синкумар (непрямой антикоагулянт) или сулодексид (комплекс глюкозаминог ликанов). При лечении антиагрегантами и антикоагулянтами необходимо добиться исчезновения признаков гиперкоагуляции (нормализация АЧТВ, тромбинового времени, протробиновый индекс должен быть снижен до 60–75 %).
Терапия гиперкоагуляционного синдрома при гематогенных тромбофилиях: при тромбозах на фоне дефицита антитромбина III назначают в/в введение очищенных препаратов антитромбина III, а при их отсутствии – большие объемы свежезамороженной плазмы (1–1,5 л); проводится терапия антиагрегантами и непрямыми антикоагулянтами (синкумар, кумадин); при дефиците протеина С показаны переливания больным препаратов протеина С. В терапии гиперкоагуляционного синдрома при гетерозиготном дефиците протеина С необходимо избегать назначения непрямых антикоагулянтов (синкумара, кумадина), так как они снижают концентрацию протеина С в крови и могут усилить тромбогенность. В этих ситуациях предпочтительно использовать низкомолекулярные гепарины, комбинации антиагрегантов (например, аспирин + тиклид или аспирин + плавикс). При наличии V фактора Leiden широко используют непрямые антикоагулянты.
Гипергомоцистеинемический гиперкоагуляционный синдром лечится небольшими дозами витаминов В12, В6, фолиевой кислоты. В терапии гиперкоагуляционного синдрома при антифосфолипидном синдроме и наличии аутоантител волчаночного типа предпочтение отдается аспирину, низкомолекулярным гепаринам и повторным процедурам лечебного плазмафереза. При синдроме "липких тромбоцитов" необходимо добиться блокады агрегации тромбоцитов. С этой целью применяют антиагреганты, часто их комбинации: аспирин + тиклид, аспирин + плавикс. При проведении агрегатометрии в целях контроля эффективности терапии необходимо зафиксировать феномен дезагрегации тромбоцитов в ответ на добавление ристоцетина и АДФ. При повышении уровня фактора VIII и фактора Виллебранда гиперкоагуляционный синдром купируется путем сочетания медикаментозных и экстракорпоральных методов терапии. Часто назначаются низкомолекулярные гепарины или непрямые антикоагулянты (синкумар, кумадин), антиагреганты в сочетании с обычными или селективными методами плазмафереза.
Гиперкоагуляционный синдром при травматизации и разрыве целостности сосудистой стенки в первую очередь требует остановки кровотечения и местного гемостаза. Так как этот тип гиперкоагуляционного синдрома легко переходит в гиперкоагуляционную фазу ДВС-синдрома, то в его терапии преимущество отдается внутривенным трансфузиям достаточных объемов свежезамороженной плазмы. Терапия гиперкоагуляционного синдрома при различных вариантах тромбоцитопений проводится дифференцированно, с учетом генеза тромбоцитопенического синдрома. При апластической анемии часто гиперкоагуляционный синдром не требует никакой коррекции. Однако при появлении кровоточивости или локальных кровотечений трансфузии концентрата тромбоцитов должны сочетаться с переливаниями свежезамороженной плазмы.
Гиперкоагуляционный синдром при опухолях отличается интенсивностью и устойчивостью к проводимой терапии. Зачастую прямые и непрямые антикоагулянты, антиагреганты дают слабый и кратковременный эффект. Этот вариант гиперкоагуляционного синдрома, как правило, купируется только после ликвидации опухолевого процесса в сочетании с антикоагулянтной и дезагрегантной терапией. Нередко таким пациентам показаны трансфузии свежезамороженной плазмы.
Гиперкоагуляционный синдром при гемолизе требует адекватной терапии гемолитического процесса (стероидные гормоны, цитостатики, спленэктомия и др.). Иногда определенной эффективностью обладают дезагреганты – курантил, трентал.
Поскольку гиперкоагуляционные синдромы могут длиться часы, дни, недели, месяцы и даже годы, продолжительность и варианты их терапии определяются в каждом конкретном случае индивидуально и иногда носят пожизненный характер. При выявлении ДВС-синдрома показан перевод больного в реанимационное отделение, при необходимости – подключение ИВЛ. Необходимо воздействовать на причины возникновения ДВС (антибактериальная терапия при сепсисе).
Коррекция гемостаза. В фазе гиперкоагуляции при отсутствии активного кровотечения вводят гепарин в/в медленно в изотоническом растворе хлорида натрия 1000 ЕД в час. Свежезамороженная плазма – минимум 1000 мл в/в быстрой инфузией под контролем центрального венозного давления. В стадии гипокоагуляции – трансфузии свежезамороженной плазмы 1000 мл и более до достижения нормокоагуляции, повторяя трансфузии каждые 6–8 ч. При геморрагическом синдроме, сочетающемся с тромбоцитопенией, показано введение тромбоцитной массы. При восстановлении объема крови физиологическим раствором следует опасаться перегрузки системы кровообращения, отека легкого. Коррекция газового состава крови: подача кислорода, введение растворов гидрокарбоната натрия. Для улучшения почечного кровотока при гипотонии – субинотропные дозы допамина; растворенный в 5 %-ном растворе глюкозы до 0,05 %-ной концентрации препарат вводят с начальной скоростью 1–5 мкг/кг/мин. При развитии почечной недостаточности – гемодиализ. Для снижения концентрации иммунных комплексов, продуктов фибринолиза, бактериальных токсинов показан плазмаферез.
Профилактика повторного возникновения ДВС состоит в ликвидации или предупреждении возникновения условий, которые провоцируют ДВС (лечение основного заболевания, введение гепарина при гиперкоагуляции, повторные трансфузии СЗП).
Лечение острой массивной кровопотери. Стратегическими принципами трансфузионной терапии острой массивной кровопотери, как правило сочетающейся с ДВС-синдромом, являются восстановление органного кровотока (перфузии) путем достижения необходимого объема циркулирующей крови, поддержание уровня факторов свертывания в количествах, достаточных для гемостаза, с одной стороны, и противостояния избыточному диссеминированному свертыванию – с другой, восполнение количества циркулирующих эритроцитов (переносчиков кислорода) до уровня, обеспечивающего минимально достаточное потребление кислорода в тканях. Используются солевые растворы, коллоиды (альбумин, препараты гидрооксиэтил-крахмала, желатины и декстраны), компоненты крови – СЗП, эритроциты, тромбоциты, криопреципитат.
Каждый переливаемый компонент крови решает свою специфическую задачу. Переливание СЗП необходимо для восполнения или предупреждения дефицита плазменных факторов свертывания при остром ДВС-синдроме – развившемся или неминуемо ожидаемом вследствие планируемой обширной операции. Эритроциты переливают при появлении признаков кислородной недостаточности (одышка, тахикардия). Тромбоциты назначают при необходимости восполнения развившейся тромбоцитопении потребления или дилюционной тромбоцитопении, когда их уровень нерезко снижен (менее 100 · 10/л), но их агрегационная способность нарушена из-за ДВС-синдрома и имеет место тромбоцитопеническая петехиальная кровоточивость.